Hidronefrosis
Febrero 2013
Antenatally diagnosed hydronephrosis: current postnatal management
Michael T. Davenport
Pediatr Surg Int (2013) 29:207–214
Introducción
Aproximadamente 1% de las ecografías del
screening prenatal detectan anomalías fetales. De ellas, las anomalías
genitourinarias representan 20% de las anomalías detectadas. La
hidronefrosis prenatal (ANH), definida como dilatación del sistema colector
renal fetal, afecta entre 1 - 5% de embarazos.
El diagnóstico diferencial de hidronefrosis prenatal es amplio e incluye
obstrucción de unión ureteropélvica, reflujo vesicoureteral y valvas uretrales
posteriores. Si estas patologías no se tratan pueden causar morbilidad postnatal
como litiasis renal, infección tracto urinario, cicatrización renal, pérdida
renal y enfermedad renal crónica. El diagnóstico precoz y investigación
postnatal de estas anomalías pueden reducir la morbilidad.
La gran mayoría de ANH es transitoria y se resuelve espontáneamente sin intervención o complicación y por tanto es benigna. La hidronefrosis representa un espectro y se debe distinguir qué casos de hidronefrosis presentan el mayor riesgo para el desarrollo postnatal de patología y requiere seguimiento y potencial intervención. El asesoramiento adecuado y la educación a padres es fundamental en las decisiones de investigar y tratar su hijo con ANH.
Este trabajo se basa en patología del tracto superior en relación con obstrucción de unión pieloureteral dado que es muy extenso revisar todas las causas de ANH
Historia natural de hidronefrosis prenatal.
Detección prenatal de ANH
Ecografía prenatal se realiza a 18-20
semanas de gestación. Parámetro más usado para presencia y severidad de
ANH en screening prenatal es el diámetro antero-posterior (APD) de pelvis renal.
No hay aún valor predeterminado de APD que discrimine ANH patológica de benigna.
Establecer este umbral es difícil pues APD varía con varios factores incluyendo
edad gestacional y estado de hidratación materna.
Muchos estudios han medido APD en ecografía prenatal para predecir postnatal patología.
Ismaili y cols estudió prospectivamente 213 nińos :
Encontró que corte de APD de 10 mm en tercer trimestre detecta 23% de anomalías renales.
Un punto de corte APD de 7 mm en misma cohorte detectó 68% de anormalidades
Ello sugiere que punto de corte APD inferior proporciona mayor sensibilidad en detección de patología.
Coplen y cols evaluaron cohorte de 257 recién nacidos con hidronefrosis detectada prenatalmente y encontraron que punto de corte de 15 mm detectó patología renal en 80% de fetos con sensibilidad de 73% y especificidad 82%.
Clasificación de hidronefrosis antenatal
La clasificación de ANH según severidad ayuda a estimar riesgo potencial de patología y a orientar la toma de decisiones clínicas. Varios sistemas de gradación se han utilizado para clasificar ANH pero todos son subjetivos y con variabilidad inter-proveedor. Por eso se objetiva con el APD.
Lee y cols, meta-análisis de 17 estudios y total 1.308 pacientes con hidronefrosis antenatal estratificaron ANH según tamańo APD en ecografía prenatal. Su análisis encontró diferencia en umbral de APD según edad gestacional.
ANH leve : APD ≤ 7 mm en segundo trimestre y APD ≤ 9 mm en tercer trimestre.
ANH severa : APD ≥ 10 mm en segundo trimestre y APD ≥ 15 mm en tercer trimestre.
Solo rara vez la hidronefrosis antenatal progresó con tal rapidez que requiriera intervención fetal para liberar obstrucción urinaria.
Estudios animales muestran que obstrucción urinaria no sólo causa displasia renal e insuficiencia renal sino tambien oligoamnios e impedimento de desarrollo pulmonar normal. Actualmente intervención como cirugía fetal abierta, vesicocentesis ó aspiración pelvis renal, se reserva para fetos con rińón único e hidronefrosis severa y oligohidramnios ó fetos con valvas uretrales posteriores y oligohidramnios. Intervención sólo se recomienda en segundo y tercer trimestre del embarazo y conlleva morbilidad y mortalidad que limita su utilidad.
Otras características importantes en determinar la gravedad de ANH son dilatación de cálices y adelgazamiento del parénquima renal.
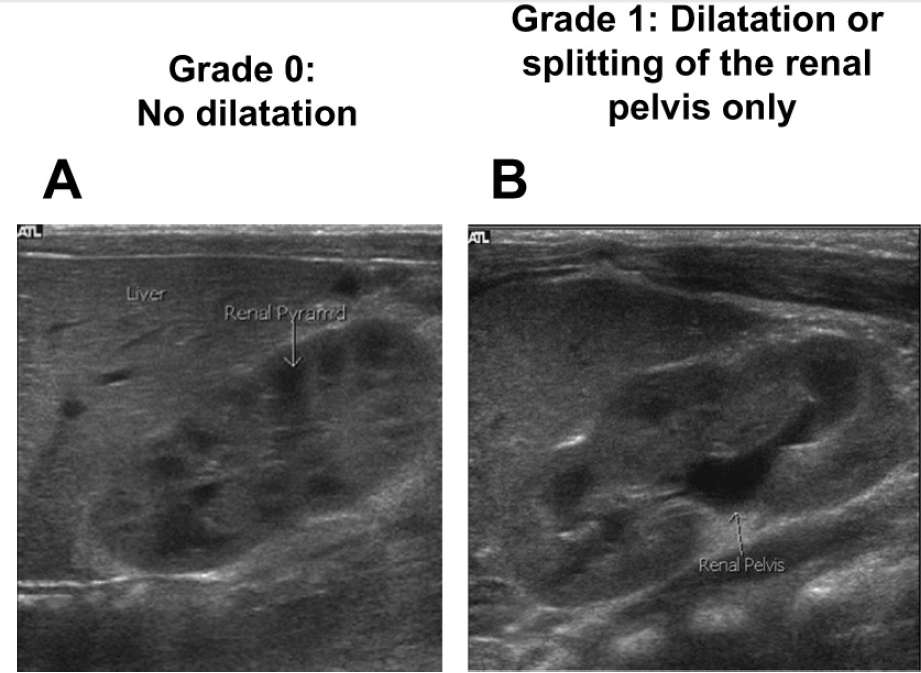
La Sociedad de Urología Fetal (SFU) considera estos factores para su clasificación (Figura 1). Considera escala de cinco puntos :
Grado 0 : ecografía renal normal
Grado 1 : inicio de hidronefrosis
Grado 4 : dilatación de pelvis y cálices mayores, además de adelgazamiento del parénquima

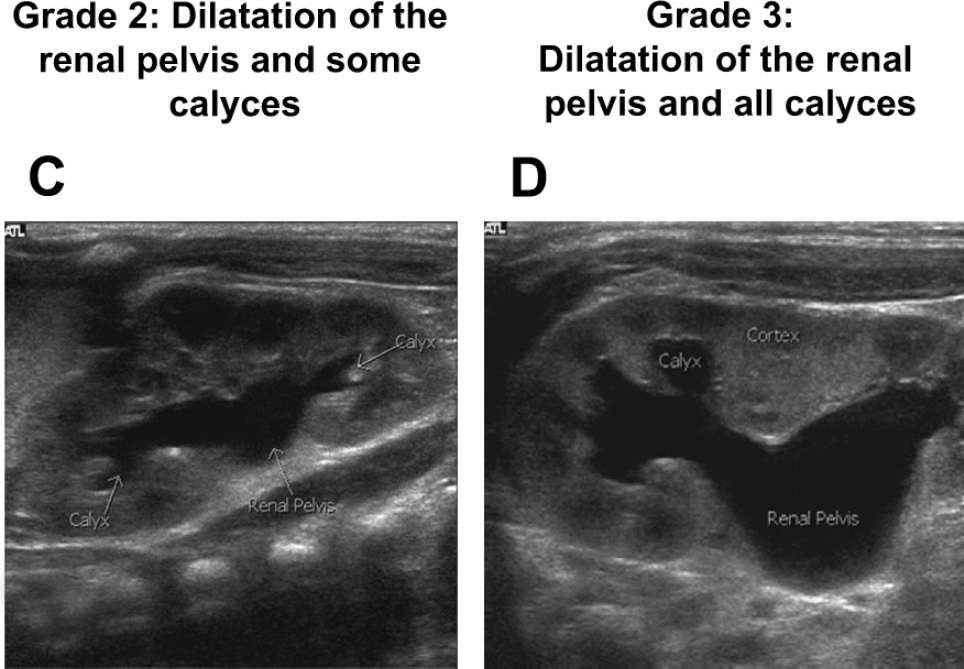
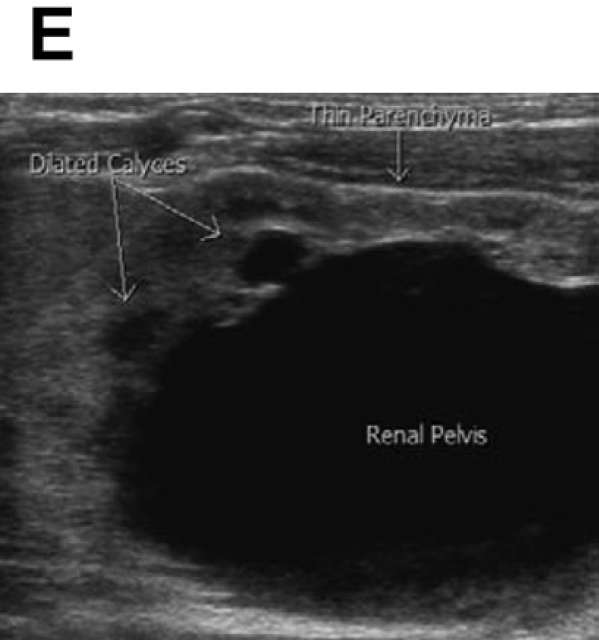
Grado 4 : dilatación de pelvis renal y cálices + adelgazamiento parénquima renal.
Outcomes a largo plazo
Thomas. J Pediatr Urol, 2010, 6:204 : cohorte de 76 nińos con ANH , todos tenían función renal significativa >
40% y se observaron durante mínimo de 16 ańos. De estos 76 nińos :52% presentaron resolución significativa ó completa de hidronefrosis y sin recidiva en período de seguimiento.
11% tenían hidronefrosis estable durante todo el período de seguimiento sin complicaciones o intervención.
37% se sometió a pieloplastia por aumento en dilatación, disminución de función diferencial ó inicio de síntomas tales como infección
Ulman y cols , siguieron 104 recién nacidos con ANH severa , unilateral :
23 nińos requirieron cirugía.
De nińos restantes :
69 % experimentó resolución espontánea de hidronefrosis en período de seguimiento precoz < 2,5 ańos.
31 % hidronefrosis persistente pero en mejoría en este mismo período de seguimiento.
De los nińos que tenían disminución de función diferencial < 40%, 24% tenían mejora en función a una media de 47% en 18 meses.
Ismaili y cols , datos retrospectivos, cohorte 234 recién nacidos con hidronefrosis detectada prenatalmente en período hasta 13 ańos :
22% requirió pieloplastía por disminución de función.
182 nińos restantes fueron manejados de forma conservadora con observación
137 se encontró que tenían función renal estable ó mejorada.
Pieloplastia retrasada en 45 de 182 recién nacidos por disminución de función diferencial ó ITU a edad media de 18 meses .
Observación versus Intervención precoz
La mayoría de los nińos con hidronefrosis diagnosticada prenatalmente tendrán resolución espontánea de la dilatación ó permanecen asintomáticos con dilatación persistente.
Aproximadamente 25-33% de los casos empeoran en el transcurso de la observación con función renal disminuída o infección y requieren intervención quirúrgica.
Es imprescindible diseńar una estrategia de manejo que evite el sobreuso de cirugía innecesaria, pero que sea lo suficientemente sensible como para detectar casos de disminución de función.
La Sociedad de Urología Fetal (SFU) y la Asociación Urológica canadiense (CUA) han hecho recomendaciones para orientar a los clínicos pero hay división con respecto a la interpretación de los datos disponibles.
Antibióticoprofilaxis
Los nińos con ANH son tratados con profilaxis antibiótica para prevenir infección del tracto urinario y dańo renal potencial por pielonefritis. Hasta la fecha, no ha habido estudios prospectivos randomizados que evalúen la utilidad de profilaxis antibiótica en nińos con ANH. Existen múltiples estudios retrospectivos conflictivos mostrando algunos mayor riesgo de infección del tracto urinario y otros no, y el tema sigue siendo controvertido.
Un análisis retrospectivo de cohorte por Walsh cols reportó que nińos con hidronefrosis tenían 12 veces más probabilidades de ser hospitalizados por pielonefritis en el primer ańo de vida en comparación con nińos sin hidronefrosis.
Otros grupos han encontrado resultados similares en su análisis y también demuestran que el riesgo de infección aumenta con el grado de hidronefrosis.
En análisis de cohorte de 192 recién nacidos con ANH, Coelho ycols encontraron que incidencia de infección asociada con hidronefrosis leve, moderada y severa fue 11, 18 y 36%, respectivamente, a la edad de 36 meses.
Lee cols encontraron resultados similares indicando que tasa de infección era 40% en recién nacidos con hidronefrosis grado 4 SFU, incluso cuando se controla por reflujo.
En ambos estudios las infecciones del tracto urinario fueron diagnosticados por muestras de orina en recolectores lo que puede haber sobre estimado la incidencia de infección del tracto urinario.
Hay igual número de estudios que muestran un bajo riesgo de infecciones del tracto urinario en nińos con ANH sin reflujo vesicoureteral.
Estrada y cols centraron análisis en 1.514 de 2.076 con ANH con hidronefrosis grado 2 que fueron estudiados para RVU con cistouretrografía miccional. De 828 pacientes que no tenían reflujo, sólo 11 ó 1,3% tuvo finalmente ITU.
Centrándose en 92 pacientes con hidornefrosis grado 3 ó 4 hidronefrosis sin reflujo, Roth y cols encontraron antecedentes de infección urinaria en sólo 4,3% de nińos. Los datos de este estudio muestran una tasa ligeramente más alta de ITU , 8,3%, en nińos con hidrouréter, pero sigue siendo inferior a los estudios anteriores.
La Asociación Urológica canadiense (CUA) reconoce la ambigüedad que rodea el tema y sólo confiere una recomendación grado D para el uso de profilaxis antibiótica en hidronefrosis sin reflujo . Por el contrario, la SFU ha redactado recomendaciones para uso de antibióticos profilácticos en todos los casos de hidronefrosis, excepto para la más leve. La SFU recomienda uso de antibióticos en nińos con factores de riesgo adicionales para ITU como hidrouréter y reflujo [2]. Estas guías reconocen que el uso de antibióticos no está exento de riesgos, incluyendo varios efectos secundarios, como reacciones alérgicas, desarrollo de resistencia bacteriana y mayor riesgo de infecciones por hongos.
Dada la incertidumbre de datos disponibles, la decisión de iniciar profilaxis con antibióticos debe ser hech considerando cuidadosamente los riesgos potenciales y beneficios.
Circuncisión
La Academia Americana de Pediatría aumentó su apoyo a circuncisión ante la evidencia de prevención de infección del tracto urinario, transmisión del VIH y cáncer de pene, pero no recomienda circuncisión de rutina para todos los recién nacidos. Varios estudios han demostrado que circuncisión puede prevenir infección del tracto urinario en caso de reflujo y valvas uretrales posteriores (PUV).
Mukherjee y cols realizaron análisis transversal retrospectivo de 78 pacientes no circuncidados con PUV. De estos nińos, 27 fueron circuncidados y experimentaron una reducción del 83% en incidencia de infección urinaria en comparación con nińos no circuncidados. El estudio también encontró que el NNT (nş necesario para tratar) para prevención de ITU con circuncisión en nińos con VUP es cercano a 1, en comparación con 111 para nińos con anomalías GU.
Herndon et al. encontraron resultados similares en estudio multicéntrico de nińos con reflujo vesicoureteral. Analizaron 56 nińos, 37 circuncidados y 19 no circuncidados. Los no circuncidados tenían mayor incidencia de infección, odds ratio de 4,0, con 35% que presentaron ITU a pesar de antibióticos profilácticos versus 19% de nińos circuncidados.
Los datos para nińos con hidronefrosis sin hidrouréter ó PUV son menos numerosos. Roth y cols analizaron nińos con hidronefrosis grados 3 y 4 y mostraron que ninguno de los nińos circuncidados desarrolló ITU en comparación con 8,3% de varones no circuncidados que desarrollaron infección.
Los datos sugieren que nińos con cualquier grado de hidronefrosis se beneficiarían con circuncisión. Sin embargo, estudios son todos retrospectivos y hasta la fecha, no hay estudios prospectivos randomizados para comprobar la utilidad de circuncisión.
Ecografía renal
La ecografía renal es importante para evaluación de nińos con ANH en fases inicial y seguimiento de atención. Como screening la ecografía permite diferenciar la enfermedad de bajo y alto riesgo en base a criterios de clasificación SFU 0-2 y 3-4, respectivamente.
Pacientes de bajo riesgo requieren imagenología de seguimiento a intervalos y dada la ausencia de radiación, la facilidad de uso y no invasividad, esto se realiza por ecografía. Los datos muestran que monitoreo con criterios SFU y la medición de APD puede ayudar a predecir qué pacientes requieren intervención quirúrgica y guiar tratamiento adicional.
La gran mayoría de ANH se detecta durante segundo trimestre de embarazo dado que screning ecográfico se hace a las 20 semanas de gestación. Los hallazgos anormales en esta ecografía inicial son entonces seguidos con ecografías prenatales seguidas durante el tercer trimestre y con ecografía renal durante período postnatal.
La ecografía renal no tiene radiación, relativamente fácil de usar y fácilmente accesible. Pero no está exenta de defectos. Hay un alto grado de variabilidad entre operadores en habilidad e interpretación lo que puede disminuir el valor predictivo. Además, el estado de hidratación del RN también puede afectar la capacidad de ecografía para predecir la patología.
Al nacer, los RN están relativamente deshidratados y por tanto, una ecografía realizada inmediatamente después del nacimiento puede subestimar grado de hidronefrosis. Por lo tanto SFU y CUA recomiendan posponer la ecografía renal postnatal inicial hasta al menos 1 semana de vida a menos que se requiera por síntomas tales como infección febril ó aumento de creatinina. Estas mismas guías proponen mayor vigilancia en nińos con factores adicionales de riesgo de dańo renal, incluyendo hidronefrosis bilateral severa y cualquier grado de hidronefrosis en rińón único, recomendando realizar antes del alta del hospital al nacer.
La ecografía es screening que puede determinar la necesidad de realizar más estudios para evaluar la necesidad de intervención quirúrgica. Ecografías asociadas pueden determinar progresión de dilatación y disfunción renal. La CUA recomienda uso de ecografía en combinación con criterios de clasificación SFU para clasificar a pacientes en grupos de observación y casos que requieren evaluación adicional.
La hidronefrosis grados 0-2 SFU puede observarse estrechamente con imagen anual para detectar empeoramiento de hidronefrosis, pero enfermedad más severa, grados 3-4, a menudo requieren un estudio diagnóstico más amplio.
Dhillon y cols reportan que medición de APD puede ayudar a predecir la necesidad de intervención quirúrgica, siguiendo prospectivamente 139 unidades renales con función diferencial > 40% durante un período de 6 a 13 ańos con tratamiento conservador. Para rińones con APD entre 30 y 40 mm, 21 de 25, finalmente requirieron cirugía para corregir obstrucción. Adicionalmente, siguieron 36 rińones con APD > 40 mm y encontraron que todos ellos requirieron corrección quirúrgica.
Cistouretrograma miccional
Cistouretrograma miccional (CUM) se usa en evaluación de nińos con ANH para detectar reflujo vesicoureteral y patología del tracto inferior, tal como valvas uretrales posteriores, ureteroceles ó divertículos vesicales. Sin embargo, dado que la gran mayoría de casos se resuelven ó permanecen asintomáticos ha impulsado un nuevo debate sobre la utilización de CUM. Tanto Sociedad de Urología Fetal y Asociación Urológica canadiense (CUA) han recomendado que a todos los casos de ANH con ecografía renal que muestre SFU dilatación grado 4 se les haga CUM para descartar reflujo y otras posibles patologías. Tambien recomiendan CUM sea aplazada en casos menos graves de ANH : grados 0-2 SFU, dado que CUM es más invasiva que ecografía y en estos nińos no se mostrado que progresen a patología significativa. Sin embargo dichas recomendaciones son equívocas, cuando cicatrización con ANH grado 3 SFU ya que este grupo de rińones tiene los datos más contradictorios con respecto a progresión de patología.
Debido a esta ambigüedad, se recomienda que se adopte un enfoque más individualizada con estos pacientes y la decisión de realizar CUM se haga caso a caso y con la participación de padres en toma de decisiones. Factores que podrían influir en decisión de recomendar CUM incluyen hallazgos que sugieren enfermedad del tracto urinario inferior, como valvas uretrales posteriores. Estos hallazgos incluyen hidronefrosis bilateral, uréter dilatado, rińones duplex, ecogenicidad renal anormal y apariencia anormal de vejiga.
Cintigrafía renal
En evaluación de pacientes con ANH, cintigrafía renal puede ofrecer información útil para planificar tratamiento adicional incluyendo estimación de función renal y diagnóstico de patología obstructiva. Sin embargo, como con Cistouretrografía miccional el uso de cintigrafía renal sigue siendo controvertido debido a su naturaleza invasiva, costo y exposición a radiación. Hay varios diferentes radiofármacos - incluyendo Tc-MAG 3, Tc- DTPA y Tc-DMSA - para realizar exploración renal. De estos tres isótopos, Tc-MAG3 se ha convertido en el más utilizado ya que proporciona mejor definición del parénquima y sistemas colectores para estimar mejor la función renal y requiere menos exposición a radiación.
Se puede realizar sin sedación ó anestesia en el paciente muy joven. Hidratación, distensión vesical, capacidad y función para responder a furosemida son todos parámetros importantes en la evaluación de drenaje. De hecho, muchos profesionales buscan más perfusión inicial ó datos de la función, que curvas de respuesta a diurético.
En pacientes con enfermedad de bajo riesgo, grados 0-2 SFU , gammagrafía renal se debe realizar cuando observación ó aumento de síntomas muestran progresión de hidronefrosis.
Para hidronefrosis grado 4 SFU y Cistouretrografía miccional sin reflujo, se recomienda una gammagrafía renal MAG 3 para determinar la función renal y el drenaje. Si hay reflujo y sobre todo si es de alto grado un scan DMSA puede ser beneficioso dado que mayoría de estos nińos tienen displasia renal.
Para hidronefrosis grado 3 el manejo debe ser individualizado. Se recomienda ecografía seriada y reservar scan MAG 3 para aquellos sin reflujo y con hidronefrosis persistente ó en aumento. Dado que la fase diurética de gammagrafía renal MAG 3 no es segura en determinar obstrucción la indicación absoluta de intervención quirúrgica recomendada por la SFU es una disminución de la función renal diferencial a < 40%. Otras indicaciones para cirugía incluyen aumento de hidronefrosis en el seguimiento con drenaje retardado en cintigrafía renal.
Resumen
Hidronefrosis prenatal es la anomalía más frecuentemente diagnosticada en ecografía prenatal. Meta-análisis ha mostrado que estos nińos tienen un mayor riesgo de patología postnatal en comparación con nińos dentro de población normal. Sin embargo, grado de este riesgo, al igual que severidad de hidronefrosis, varía en gran medida entre nińos.
Históricamente, mayoría de nińos con hidronefrosis prenatal fueron manejados quirúrgicamente para evitar posibles outcomes adversos, como infección e insuficiencia renal. Recientemente, sin embargo, esta práctica se ha vuelto menos común, dado que datos de seguimiento a largo plazo ya mostrados han comenzado a sugerir que la mayoría de nińos permanecen asintomáticos con hidronefrosis estable ó en resolución.
Nuestro estudio también evalúa los datos disponibles sobre sensibilidad y especificidad de varias técnicas de imagen en predecir hidronefrosis antenatal patológica.
Si bien cada nińo en última instancia, debe ser manejado de forma individual, estos datos proporcionan un marco ideal sobre el cual basar las guías de manejo para nińos con hidronefrosis prenatal.
Recomendaciones
Grado 0 – 2 SFU
Datos a largo plazo indican que nińos con hidronefrosis prenatal de bajo grado tienen resolución de dilatación ó permanecen estables sin complicación patológica en mayoría de los casos. En consecuencia, la intervención quirúrgica inicial no está indicada ni recomendada ni por la SFU ni CUA.
Debe iniciarse un protocolo de manejo expectante para monitorizar cualquier progresión de la dilatación ó desarrollo de síntomas que pueden conducir a futuro dańo renal tales como fiebre.
De acuerdo con recomendaciones de SFU y CUA, todos los nińos con hidronefrosis diagnosticada prenatalmente deben tener una ecografía renal poco después del nacimiento, pero no antes de las 2 semanas de vida para evitar la fase diurética postnatal inicial.
Grado 3 SFU
Recomendamos profilaxis antibiótica hasta completar los estudios, sobre todo si familia decide hacer Cistouretrografía miccional (CUM) . La ecografía se debe realizar a los 7-14 días después del nacimiento . Se debe aconsejar a la familia realizar CUM para evaluar el reflujo. Si CUM es negativo para reflujo recomendamos suspender profilaxis antibiótica.
Si no se realiza CUM se debe asesorar a la familia para tomar decisión después de proporcionar datos disponibles, respetando su decisión.
La circuncisión también debe ser una decisión basada en modelos similares.
Recomendamos repetir ecografía alrededor de los 3 meses de edad y si el grado de hidronefrosis se mantiene igual ó empeora, se debe realizar una cintigrafía renal diurética Tc-MAG 3.
Grado 4 SFU
Realizar profilaxis antibiótica hasta completar estudios. Si existe dilatación ureteral, debe realizrse CUM. Si CUM no muestra reflujo puede suspenderse antibióticos, aún sabiendo que datos retrospectivos sugieren un aumento del riesgo de ITU en este grupo de nińos.
Los nińos con hidronefrosis grado 4 tienen las anomalías renales más graves y como se muestra en datos de seguimiento a largo plazo, el mayor riesgo para el desarrollo de patología renal. Estos datos también muestran que estos nińos requieren intervención quirúrgica más a menudo para prevenir tales eventos adversos.
Al igual que con todos los recién nacidos con ANH se recomienda que ecografía renal sea realizada después de 2 semanas de vida para reevaluar la dilatación renal.
Debido al riesgo aumentado de outcomes patológicos en estos nińos, debe indicarse CUM . Si se encuentra reflujo vesicoureteral debe indicarse scanner DMSA en casos seleccionados con el fin de evaluar la función diferencial.
Si CUM es negativa para reflujo se debe realizar renograma diurético para aclarar etiología de hidronefrosis y hacer plan para posible tratamiento quirúrgico.
Debido a que datos respecto a profilaxis antibiótica y circuncisión en nińos con ANH son conflictivos recomendamos que sean reservados para casos sintomáticos
Hidrouréter
En este grupo de pacientes, el riesgo de desarrollar infección del tracto urinario es mayor que en nińos con dilatación limitada al rińón. Por tanto, mayor cuidado se debe tener para proteger contra dańo renal. Se recomienda que a estos nińos se les realize imagenología dentro de los primeros 7 días, incluyendo al menos ecografía renal.
A estos pacientes se les debe indicar profilaxis antibiótica hasta que estudios de imagenología estén completos debido a mayor riesgo de infección.
Hidronefrosis bilateral
Como en el caso hidrouréter, hay nueva evidencia que sugiere que nińos con hidronefrosis bilateral pueden beneficiarse de evaluación precoz y profilaxis antibiótica. Los nińos con enfermedad bilateral tienen mayor riesgo de infección en comparación con hidronefrosis unilateral. Este riesgo también aumenta con el grado de hidronefrosis teniendo la hidronefrosis bilateral severa mayor incidencia de infección que casos más leves.
Por tanto, se recomienda que a estos nińos se les indique profilaxis antibiótica a la espera de completar los estudios.
Hidronefrosis bilateral no solo conlleva un aumento del riesgo de infección, sino también puede ser un signo de patología subyacente más severa como valvas uretrales posteriores en nińos.
Por lo tanto, se recomienda que estos nińos sean evaluados con ecografía y potencialmente CUM antes de ser dados de alta del hospital después del nacimiento
Referencias