Prueba de pagina o modela a usar
Noviembre 2005
Efectividad de la terapia con leuprolide acetato de depˇsito cada tres meses en pubertad precoz central
M Verˇnica Mericq G1, Ronald Youlton R1, M Eugenia Willshaw Z2.
1Departamento de PediatrÝa, Unidad de EndocrinologÝa, ClÝnica Las Condes y 2Departamento de PediatrÝa, Hospital Militar de Santiago, Santiago, Chile.
Rev. mÚd. Chile v.134 n.7 Santiago jul. 2006, 821 - 826
En el ßmbito mundial, existe evidencia sobre una tendencia secular al adelanto de la edad de la pubertad, particularmente en el sexo femenino. En Chile existe informaciˇn desde hace poco mßs de cien a˝os, como tambiÚn estudios recientes1. Esta observaciˇn ha llevado a la Lawson Wilkins Pediatric Endocrine Society a descender los lÝmites de edad en que se considera normal la iniciaciˇn de la pubertad en Estados Unidos de NorteamÚrica (EE.UU)2. Sin embargo, el consenso de un grupo de expertos en nuestro paÝs, ha sugerido, por el momento, mantener el criterio de diagnˇstico de pubertad precoz como aquella que se inicia antes de los ocho a˝os en ni˝as y nueve a˝os en varones. Esta decisiˇn se ha tomado considerando que, al menos, la edad de menarquia ha sido estable en los ˙ltimos 30 a˝os y en varones no se demostrˇ un adelanto en la edad de inicio puberal3. Las consecuencias de un desarrollo puberal anticipado son la pÚrdida de centÝmetros de estatura final por fusiˇn temprana de los cartÝlagos de crecimiento y la eventual presentaciˇn de problemas emocionales y psicolˇgicos.
Actualmente existe consenso sobre la utilizaciˇn de anßlogos agonistas superactivos del factor liberador hipotalßmico de gonadotrofinas (aLHRH), en los casos de pubertad precoz central. Las base fisiolˇgica del tratamiento deriva de las observaciones de Knobil, que demostraron que la estimulaciˇn pulsßtil de la hipˇfisis con LHRH estimula la secreciˇn de gonadotrofinas y que la estimulaciˇn continua la inhibe4.
Los aLHRH que se utilizan tienen una mayor afinidad por el receptor de LHRH de los gonadotrofos y una mayor resistencia a su degradaciˇn enzimßtica5. Los objetivos de la terapia con aLHRH, en la pubertad precoz central, son la detenciˇn o regresiˇn de los caracteres sexuales secundarios, inhibiciˇn de los ciclos menstruales, restaurar el comportamiento apropiado a la edad cronolˇgica, restaurar el patrˇn de crecimiento y mejorar el pronˇstico de estatura. Todos estos objetivos son razonablemente alcanzables con la terapia de aLHRH6,7.
Los primeros aLHRH sintetizados se suministraban diariamente por vÝa subcutßnea o por vÝa intranasal. Posteriormente, aparecieron preparados farmacÚuticos de depˇsito, con una duraciˇn de actividad promedio de cuatro semanas. Recientemente han aparecido formulaciones de mayor duraciˇn, que permiten administrar el medicamento en forma mßs alejada. Esta caracterÝstica representa claramente una ventaja comparativa en tÚrminos de adherencia y, a veces, de costo para los pacientes. En la actualidad, existe un ˙nico reporte sobre el uso de anßlogo de LHRH cada 90 dÝas en pubertad precoz central y su efectividad en la inhibiciˇn de las gonadotrofinas durante un perÝodo de 6 meses8.
El objetivo de este trabajo fue evaluar la eficacia de un preparado de aLHRH acetato de leuprolide (Lupron« 11,25 mg) im, cada tres meses, administrado durante un periodo de 18 meses, en la supresiˇn de la activaciˇn gonadotrˇfica, signos clÝnicos de pubertad precoz y maduraciˇn ˇsea.
PACIENTES Y M╔TODOS
Once pacientes con pubertad precoz central idiopßtica, de acuerdo a los criterios auxolˇgicos actualmente vigentes en nuestro paÝs, fueron invitados a participar en el estudio. Estos pacientes fueron reclutados en el Departamento de PediatrÝa de ClÝnica Las Condes y en el Servicio de EndocrinologÝa Infantil del Hospital Militar de Santiago. Se consideraron requisitos de inclusiˇn la ausencia de tratamiento previo y clÝnicamente, el desarrollo mamario Tanner ll o mayor en ni˝as y un volumen testicular de 4 cc o mßs en varones. En forma adicional, debÝan poseer una edad ˇsea mayor que la edad cronolˇgica (>1 DS para la edad cronolˇgica), una respuesta de LH al estÝmulo de LHRH igual o superior a 5,0 UI/L9 y una concentraciˇn plasmßtica de testosterona superior a 1,7 nmol/L en varones. En todas las ni˝as se considerˇ, como criterio de ingreso, un volumen ovßrico superior a 1,5 cc, sumados a longitud uterina superior a 36 mm por ecografÝa realizada por el mismo ecografista infantil (KM). Al momento del diagnˇstico se realizˇ a todos los pacientes una tomografÝa axial computada (TAC), con contraste de cerebro y con foco hipotßlamo e hipˇfisis, con el objeto de descartar lesiones de esa zona, que secundariamente produjeran pubertad precoz.
El protocolo de estudio fue aprobado por los ComitÚs de ╔tica de ambas instituciones y, previo al inicio de la terapia, los padres firmaron un consentimiento informado.
Una vez ingresados se indicˇ el aLHRH acetato de leuprolide, en la formulaciˇn de 11,25 mg, que se inyectˇ vÝa im cada tres meses. Este producto fue gentilmente donado por Abbott Laboratorios de Chile. Los pacientes asistieron a control clÝnico cada 3 meses, donde se realizˇ un examen fÝsico completo con determinaciˇn de estatura, peso, Ýndice de masa corporal (IMC), proporciones corporales y estadio de desarrollo puberal seg˙n Tanner10. En forma adicional, se realizˇ una prueba de LHRH nativo (100 Ág/m2) en que se determinaron los niveles plasmßticos de LH y FSH a los 0, 30 y 60 min. En cada control se realizaron, ademßs, exßmenes de orina completa, perfil bioquÝmico y hemograma.
Se considerˇ que la frenaciˇn de gonadotrofinas fue adecuada cuando la concentraciˇn mßxima de LH, post estÝmulo, alcanzˇ un valor inferior a inferior a 3,0 UI/L, la de testosterona menor a 1 nmol/L (varones) y la de estradiol fue inferior a 73 pmol/L (mujeres)9. La duraciˇn del estudio fue de 18 meses (6 inyecciones).
Cada 6 meses se determinˇ la edad ˇsea en todos los pacientes mediante radiografÝa de la mano, utilizando el mÚtodo de Greulich y Pyle (informe, KM, ClÝnica Las Condes). Al mismo tiempo, se realizˇ control ecogrßfico en cada una de las ni˝as participantes. La ecografÝa ginecolˇgica fue realizada siempre por el mismo radiˇlogo (KM, ClÝnica Las Condes), utilizando un equipo ATL HDI 5000 Phillips.
Al inicio y en el control final de los 18 meses se realizˇ una densitometrÝa ˇsea de columna lumbar, utilizando un densitˇmetro marca Lunar modelo DPX alpha. El informe entrega los datos como contenido mineral ˇseo y porcentaje de adecuaciˇn para la densidad mineral areal, ambos en columna lumbar.
Se consideraron criterios de suspensiˇn lograr una predicciˇn estatural cercana (▒ 1 desviaciˇn estßndar) al pronˇstico familiar y evitar la progresiˇn del desarrollo de caracteres sexuales antes de lo considerado normal, para evitar los problemas conductuales y sicolˇgicos que se pueden observar en estas condiciones. En forma adicional tambiÚn se considerˇ criterio de exclusiˇn el presentar reacciones adversas locales en el sitio de la administraciˇn del anßlogo o en los exßmenes de laboratorio general.
Determinaciones hormonales. Todas las mediciones de LH, FSH, testosterona y estradiol fueron realizadas por electroquimioluminiscencia (ECLIA) en el Laboratorio de Hormonas de ClÝnica Las Condes. Estas determinaciones tienen un coeficiente de variaciˇn intraensayo entre 4 y 6% e interensayo entre 10 y 12%. La sensibilidad del mÚtodo para LH fue de 0,1 UI/L, para FSH de 0,1 UI/l, para testosterona de 0,069 nmol/L y para estradiol de 18 pmol/L con esta metodologÝa.
EstadÝstica. Los resultados se muestran como promedio ▒ desviaciˇn estßndar (DE). El anßlisis estadÝstico se realizˇ con el programa SPSS 10.0 para Windows. Utilizando una t de student cuando los datos se distribuyeron en forma normal y test de Wilcoxon cuando su distribuciˇn fue no paramÚtrica.
RESULTADOS
Ingresaron al estudio 11 pacientes (10 mujeres, 1 varˇn) con una edad cronolˇgica promedio de 7,5▒1,8 a˝os y edad ˇsea promedio de 9,7▒1,8 a˝os.
En las 10 ni˝as, el tratamiento se iniciˇ antes de los 9 a˝os de edad. En el varˇn se iniciˇ a los 11 a˝os. El lapso de tiempo promedio transcurrido entre los primeros sÝntomas y el inicio de la terapia fue 1,5▒0,5 a˝os.
El desarrollo mamario en las ni˝as estaba en estadios 2 a 3 de Tanner. El ˙nico paciente de sexo masculino presentaba un volumen testicular de 15 cc bilateral.
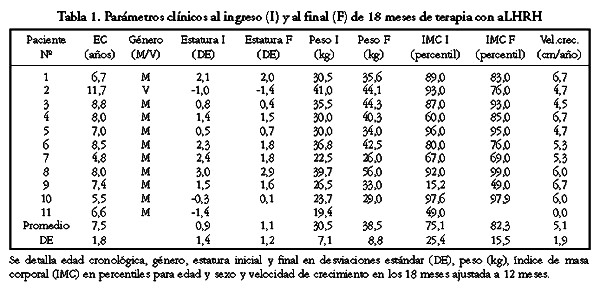
En la Tabla 1 se detallan los parßmetros clÝnicos (edad cronolˇgica, gÚnero, estatura inicial y final en desviaciones estßndar, peso [kg], IMC [percentiles para edad y sexo], velocidad de crecimiento) para cada uno de los pacientes ingresados al estudio, al ingreso (I) y al final (F) de 18 meses de terapia con aLHRH.

En el primer control clÝnico, a los tres meses de inyectada la primera dosis de acetato de leuprolide, se observˇ regresiˇn de los caracteres secundarios en todos los pacientes, con excepciˇn del vello genital. Las glßndulas mamarias redujeron su consistencia y su dißmetro en algunos casos hasta lÝmites no precisables (al ingreso 7,7▒8,2 cm versus 4,9▒3,7 cm, p <0,05), como tambiÚn el aspecto de la mucosa vaginal volviˇ a caracterÝsticas infantiles. Esto ˙ltimo no pudo ser cuantificado, pues no se hizo estudio y seguimiento de la citologÝa vaginal. AsÝ mismo, el volumen testicular del varˇn se redujo de 15 a 12 cc a los seis meses de tratamiento.
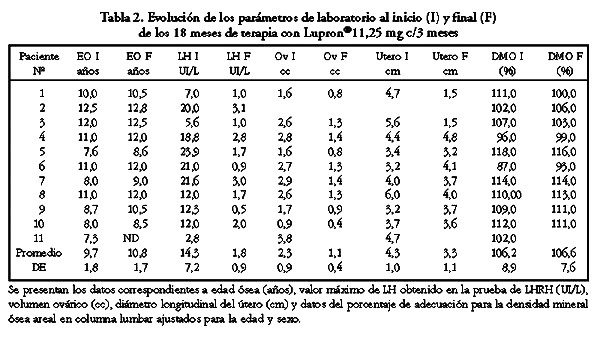
La supresiˇn gonadotrˇfica se demostrˇ a travÚs de la concentraciˇn mßxima de LH al estÝmulo de LHRH en el control del sexto mes que se encontrˇ en niveles prepuberales en todos (LH 2,05▒1,1 UI/L), excepto una paciente, en que este hecho ocurriˇ en el control siguiente. Tanto las concentraciones de estradiol en las ni˝as como la de testosterona en el varˇn disminuyeron respecto de los valores basales (estradiol basal 73,9▒48,3 pmol/L versus 44▒15 a los 3 meses y 47,7▒33 a los 18 meses y testosterona 8 nmol/l versus 0,5 nmol/L a los 3 meses y 0,2 nmol/L a los 18 meses).
Los genitales internos tambiÚn mostraron una regresiˇn rßpida. Al sexto mes el volumen ovßrico inicial de 2,3▒0,8 cc, se redujo a 1,9▒0,7 cc, diferencia que no alcanzˇ a ser significativa estadÝsticamente. La longitud uterina, sin embargo, se redujo de 4,3▒1,0 a 3,9▒0,9 cm (p <0,05).
En el seguimiento a mßs largo plazo un parßmetro importante de evaluar es la velocidad de maduraciˇn ˇsea. La edad ˇsea, inicialmente avanzada, mostrˇ una desaceleraciˇn al final del perÝodo de estudio. Esto se demuestra a travÚs del delta de edad ˇsea - edad cronolˇgica (EO-EC) que se redujo de 2,2▒1,1 a 1,7▒1,0 a˝os al final del perÝodo de 18 meses de terapia (p <0,01) lo que mejorˇ el pronˇstico de estatura inicial. Sin embargo, este ˙ltimo parßmetro es de poca utilidad con una terapia de 18 meses por lo que estos datos no se muestran.
En el aspecto antropomÚtrico, la estatura promedio inicial expresada en desviaciones estßndar (DE) para la edad y sexo en los 11 pacientes fue de 0,9▒1,4 DS. Al cabo de los 18 meses de tratamiento este puntaje cambiˇ a 1,1▒1,2 DS lo que no es una diferencia significativa. AsÝ tambiÚn, el Ýndice de masa corporal inicial (IMC) promedio estaba en el percentil 75▒25 y al final del tratamiento estaba en el percentil 82,3▒15,5 (p=NS). La informaciˇn sobre los parßmetros de laboratorio al ingreso y a los 18 meses de tratamiento con aLHRH se resumen en la Tabla 2.
En algunas ni˝as, despuÚs de la primera inyecciˇn hubo un peque˝o efecto estimulatorio inicial, pero ninguna presentˇ sangrado vaginal. Ning˙n paciente presentˇ reacciones locales en el sitio de la inyecciˇn ni se observaron efectos adversos durante el curso del tratamiento atribuibles a Úste.
Los pacientes mostraron buena adherencia al tratamiento. Sˇlo una ni˝a no concurriˇ al ˙ltimo control por cambio de residencia a un lugar alejado de Santiago.
Al momento de redactar esta comunicaciˇn, 10 pacientes acuden a control regular. Dos contin˙an el uso del anßlogo (pacientes n║ 5 y 10), un paciente completˇ 3 a˝os de terapia y tres completaron 2 a˝os de terapia. En los 8 pacientes que ya suspendieron el aLHRH se ha documentado la reactivaciˇn del eje gonadotropo.
En el paciente varˇn, esto se ha documentado con testosteronas matinales (˙ltimo valor, 15,6 nmol/L) y aumento de volumen testicular a 25 cc al a˝o posterior a suspensiˇn del anßlogo. En las ni˝as (n=7) que han suspendido el anßlogo, la menarquia ha ocurrido en 3 de 7 de ellas y este evento ocurriˇ en un lapso entre 6 y 18 meses post suspensiˇn del aLHRH. En las ni˝as restantes se ha observado un aumento progresivo del estadio de Tanner mamario asÝ como cambios estrogÚnicos en la mucosa genital.
DISCUSIËN
En esta experiencia se demuestra que el uso de acetato de leuprolide de depˇsito, en dosis de 11,25 mg, inyectado intramuscular cada tres meses es efectivo en el tratamiento de la pubertad precoz central.
ClÝnicamente todos los pacientes mostraron regresiˇn de sus signos de pubertad, lo que se acompa˝ˇ de una caÝda en la velocidad de crecimiento a niveles prepuberales y de una leve elevaciˇn del IMC.
Las gonadotrofinas hipofisiarias fueron efectivamente frenadas en 85,6▒6,9% de los valores a los tres meses de tratamiento y en 87,7▒5,1% a los 18 meses. Paralelamente, tanto los niveles de estradiol, en las mujeres, como testosterona, en el varˇn, cayeron a niveles prepuberales durante el curso del estudio. Es importante destacar que las fluctuaciones de los niveles diarios de estradiol hacen que este examen sea poco confiable como parßmetro de control de frenaciˇn de la actividad del eje gonadotropo-gonadal, por lo que es ˙til acompa˝ar la evaluaciˇn de otros Ýndices como el test de LHRH nativo y la ecografÝa pÚlvica. En los varones, sin embargo, los niveles de testosterona son muy ˙tiles, como lo demostrˇ nuestro ˙nico caso de sexo masculino, cuya concentraciˇn plasmßtica de testosterona inicial de 8,0 nmol/L se mantuvo bajˇ 0,2 nmol/L durante el tratamiento. En el estudio de Carel8, donde se utilizaron dosis similares a las nuestras, se observˇ una pobre supresiˇn de los niveles de testosterona al primer mes, posterior a la primera dosis de aLHRH. El descenso se hizo evidente al tercer mes y durante el seguimiento. Esta informaciˇn contrasta con lo reportado en adultos con cßncer de prˇstata tratados con 11,25 mg im, cada tres meses, en que se ha comunicado que las concentraciones de testosterona ya estßn adecuadamente suprimidas a las cuatro semanas de terapia11,12.
En concordancia con la frenaciˇn de gonadotrofinas y de esteroides sexuales, se demostrˇ disminuciˇn del volumen ovßrico y de la longitud del ˙tero, medidas ecogrßficamente. El volumen testicular de nuestro paciente de sexo masculino tambiÚn se redujo.
Todo lo anterior se correlaciona bien con la desaceleraciˇn de la velocidad de maduraciˇn esquelÚtica, que se confirmˇ en todos los pacientes. En sˇlo 18 meses de observaciˇn esta desaceleraciˇn fue significativa; en un periodo mßs prolongado Ústa probablemente serÝa mayor, lo cual hace que el cßlculo de proyecciˇn de estatura final no sˇlo interrumpa su deterioro sino que mejore, al menos parcialmente.
La densidad mineral ˇsea tampoco se vio afectada por el tratamiento, hecho que ha sido comunicado en otras publicaciones13. Sin embargo, este es un aspecto que en terapias mßs prolongadas podrÝa alterarse y en las cuales incluso se ha sugerido la utilizaciˇn de calcio suplementario14.
Estos datos nos sugieren que la dosis utilizada en este estudio fue adecuada para nuestros propˇsitos. Existe controversia en la literatura respecto de cußl serÝa la mßs apropiada para las formulaciones de aLHRH de 3,75 mg para uso mensual. Publicaciones europeas se˝alan que 120 Ág/kg de peso cada cuatro semanas, es decir 3,75 mg mensuales serÝan, en general, suficientes para suprimir las gonadotrofinas en ni˝os con menos de 30 kg de peso y pubertad precoz central8. Esta cantidad contrasta con las recomendaciones norteamericanas de 300 Ág/kg cada cuatro semanas15-17 y en el otro extremo las dosis que en Japˇn se utilizan. En este ˙ltimo paÝs, Tanaka ha demostrado que la dosis mÝnima efectiva es de 30 Ág/kg18.
Las reacciones locales despuÚs de inyectar aLHRH (dolor prolongado, formaciˇn de granulomas o de un absceso estÚril) ocurren en 3 a 13% de los pacientes. En ninguno de los pacientes participantes en este estudio observamos tales situaciones, como tampoco presentaron otros efectos adversos ni modificaciones en el hemograma, perfil bioquÝmico o en el examen de orina, lo que permitiˇ una buena adherencia hasta completar el estudio.
En conclusiˇn, el uso de acetato de leuprolide 11,25 mg inyectado cada tres meses ha demostrado ser efectivo y seguro para la disminuciˇn de los signos clÝnicos, frenaciˇn de gonadotrofinas y avance de la maduraciˇn ˇsea en ni˝os con pubertad precoz central. El hecho de disponer de un preparado de liberaciˇn lenta que permita ser utilizado cada tres meses favorece la adherencia a una terapia que es prolongada.
REFERENCIAS
Codner E, Unanue N, Gaete X, Barrera A, Mook-Kanamori D, Bazßes R et al. [Age of pubertal events in Chilean school age girls and its relationship with socioeconomic status and body mass index]. Rev MÚd Chil 2004; 132: 801-8.
Kaplowitz PB, Oberfield SE. Reexamination of the age limit for defining when puberty is precocious in girls in the United States: implications for evaluation and treatment. Drug and Therapeutics and Executive Committees of the Lawson Wilkins Pediatric Endocrine Society. Pediatrics 1999; 104: 936-41.
GarcÝa H, Youlton R, Burrows R, Catani A. [Consensus on the diagnosis and treatment of central early puberty]. Rev MÚd Chile 2003; 131: 95-110.
Wildt L, Marshall G, Knobil E. Experimental induction of puberty in the infantile female rhesus monkey. Science 1980; 207: 1373-5.
Okada H. One- and three-month release injectable microspheres of the LH-RH superagonist leuprorelin acetate. Adv Drug Deliv Rev 1997; 28: 43-70.
Crowley WF Jr, Comite F, Vale W, Rivier J, Loriaux DL, Cutler GB Jr. Therapeutic use of pituitary desensitization with a long-acting LHRH agonist: a potential new treatment for idiopathic precocious puberty. J Clin Endocrinol Metab 1981; 52: 370-2.
7. Klein KO, Barnes KM, Jones JM, Feuillan PP, Cutler GB Jr. Increased final height in precocious puberty after long-term treatment with LHRH agonists: the National Institutes of Health experience. J Clin Endocrinol Metab 2001; 86: 4711-6.
Carel JC, Lahlou N, Jaramillo O, Montauban V, Teinturier C, Colle et al. Treatment of central precocious puberty by subcutaneous injections of leuprorelin 3-month depot (11.25 mg). J Clin Endocrinol Metab 2002; 87: 4111-6.
Neely EK, Hintz RL, Wilson DM, Lee PA, Gautier T, Argente J et al. Normal ranges for immunochemiluminometric gonadotropin assays. J Pediatr 1995; 127: 40-6.
Marshall WA, Tanner JM. Variations in pattern of pubertal changes in girls. Arch Dis Child 1969; 44: 291-303.
Khan MS, O'Brien A. An evaluation of pharmacokinetics and pharmacodynamics of leuprorelin acetate 3M-depot in patients with advanced and metastatic carcinoma of the prostate. Urol Int 1998; 60: 33-40.
Wechsel HW, Zerbib M, Pagano F, Coptcoat MJ. Randomized open labelled comparative study of the efficacy, safety and tolerability of leuprorelin acetate 1M and 3M depot in patients with advanced prostatic cancer. Eur Urol 1996; 30 Suppl 1: 7-14; discussion 19-21.
Neely EK, Bachrach LK, Hintz RL, Habiby RL, Slemenda CW, Feezle L et al. Bone mineral density during treatment of central precocious puberty. J Pediatr 1995; 127: 819-22.
Antoniazzi F, Zamboni G, Bertoldo F, Lauriola S, Mengarda F, Pietrobelli A et al. Bone mass at final height in precocious puberty after gonadotropin-releasing hormone agonist with and without calcium supplementation. J Clin Endocrinol Metab 2003; 88: 1096-101.
Clemons RD, Kappy MS, Stuart TE, Perelman AH, Hoekstra FT. Long-term effectiveness of depot gonadotropin-releasing hormone analogue in the treatment of children with central precocious puberty. Am J Dis Child 1993; 147: 653-7.
Kaplan SL, Grumbach MM. Clinical review 14: Pathophysiology and treatment of sexual precocity. J Clin Endocrinol Metab 1990; 71: 785-9.
Parker KL, Baens-Bailon RG, Lee PA. Depot leuprolide acetate dosage for sexual precocity. J Clin Endocrinol Metab 1991; 73: 50-2.
18. Tanaka T, Hibi I, Kato K, Saito S, Shimizu N, Suwa S et al. A dose finding study of a super long-acting luteinizing hormone-releasing hormone analog (leuprolide acetate depot, TAP-144-SR) in the treatment of central precocious puberty. The TAP-144-SR CPP Study Group. Endocrinol Jpn 1991; 38: 369-76.
Correspondencia a: Dra. M. Verˇnica Mericq G. Departamento de PediatrÝa, ClÝnica Las Condes. Lo Fontecilla 441, Las Condes, Santiago. Fax: 2-4247240. E-mail vmericq@med.uchile.cl
| Rx edad ˇsea| | |
| Rx crßneo AP y L (proyecciˇn hipˇfisis)T | |
| TAC cerebral con contraste con foco en hipotßlamo e hipˇfisis | |
| EcografÝa pelviana | |
| Lubron Depot 22.5 mg (Acetato de Leuprolide) cada 3 meses | |
| Examen | Valores de referencia |
| Glucosa | |
| Hormona tiroestimulante | 0.7 - 5.7 |
| Tiroxina libre (T4) | 0.1 - 2.1 |
| Insulina | 3 - 25 |
| Testosterona | 0.17 - 0.81 |
| Estradiol (E2) pg/ml | Ver tabla |
| Hormona folÝculo estimulante mUI/ml | Ver tabla |
| Hormona l˙teo estimulante mUI/ml | Ver tabla |
| Estradiol | H folÝculo estimulante |
H l˙teo estimulante |
||
| Hombres | Hasta 43 pg/ml | 1.4 - 18.1 mUI/ml | 1.5 - 9.3mUI/ml | |
| Mujeres | Fase folicular | 13 - 166 pg/ml | 2.5 - 10.2 mUI/ml | 1.5 - 12.5 mUI/ml |
| Fase ovulatoria | 3.4 - 33.4 mUI/ml | 8.7- 76.3 mUI/ml | ||
| Fase l˙tea | 44 - 211 pg/ml | 1.5 - 9.1 mUI/ml | 0.5 - 16.9 mUI/ml | |
| Menopausia | hasta 55 pg/ml | 23- 116.3 mUI/ml | ||
| Ni˝os (1 - 10 a˝os) | Varones | Hasta 20 pg/ml | ||
| Ni˝as | Hasta 27 pg/ml |